Chuẩn kiến thức và kỹ năng
Kiến thức
– Nguyên tử gồm hạt nhân mang điện tích dương và vỏ nguyên tử mang điện tích âm ; Kích thước, khối lượng của nguyên tử.
– Hạt nhân gồm các hạt proton và nơtron.
– Kí hiệu, khối lượng và điện tích của electron, proton và nơtron.
Kĩ năng
– So sánh khối lượng của electron với proton và nơtron.
– So sánh kích thước của hạt nhân với electron và với nguyên tử.
Trọng tâm
– Nguyên tử gồm 3 loại hạt: p, n, e (kí hiệu, khối lượng và điện tích)
Hướng dẫn thực hiện
– Dùng TN vật lí hoặc mô phỏng về cấu tạo nguyên tử (sự bắn phá của hạt anpha qua một lá kim loại) để thấy: nguyên tử có cấu tạo rỗng gồm hạt nhân tích điện dương ở tâm và xung quanh có các electron tích điện âm tạo nên vỏ nguyên tử.
– Hạt nhân gồm proton tích điện dương và nơtron không mang điện
– So sánh khối lượng, kích thước của p, e, n với nguyên tử để thấy: p, e, n có kích thước vô cùng nhỏ và nguyên tử có cấu tạo rỗng, khối lượng nguyên tử hầu như tập trung ở hạt nhân.
(khối lượng tính theo đơn vị u, kích thước tính theo đơn vị )
Bài 2: HẠT NHÂN NGUYÊN TỬ – NGUYÊN TỐ HÓA HỌC – ĐỒNG VỊ
Chuẩn kiến thức và kỹ năng
Kiến thức
– Nguyên tố hoá học bao gồm những nguyên tử có cùng số đơn vị điện tích hạt nhân.
– Số hiệu nguyên tử (Z) bằng số đơn vị điện tích hạt nhân và bằng số electron có trong nguyên tử.
– Kí hiệu nguyên tử : là kí hiệu hoá học của nguyên tố, số khối (A) là tổng số hạt proton và số hạt nơtron.
– Khái niệm đồng vị, nguyên tử khối và nguyên tử khối trung bình của một nguyên tố.
Trọng tâm
– Đặc trưng của nguyên tử là điện tích hạt nhân (số p) Þ nếu có cùng điện tích hạt nhân (số p) thì các nguyên tử đều thuộc cùng một nguyên tố hóa học, khi số n khác nhau sẽ tồn tại các đồng vị.
– Cách tính số p, e, n và nguyên tử khối trung bình
Kĩ năng
– Xác định số electron, số proton, số nơtron khi biết kí hiệu nguyên tử ngược lại.
– Tính nguyên tử khối trung bình của nguyên tố có nhiều đồng vị.
Hướng dẫn thực hiện
– Nêu quy tắc trung hòa điện tích để thấy: nguyên tử trung hòa điện nên
“Số đơn vị điện tích hạt nhân (Z) = số p = số e”.
– Nguyên tử gồm 3 loại hạt: p, n, e;
Số khối của hạt nhân (A) = Z + N (số nơtron)”
– Nguyên tử khối là khối lượng tương đối của nguyên tử.
So sánh khối lượng e với khối lượng một nguyên tử để thấy: electrron có khối lượng nhỏ hơn rất nhiều (không đáng kể) so với khối lượng nguyên tử nên có thể coi nguyên tử khối xấp xỉ số khối của hạt nhân.
Þ nếu biết Z và A sẽ tính được số p, số e, số n. Áp dụng tính số p, e, n của một số nguyên tử
– Nguyên tố hóa học là những nguyên tử có cùng số p và được kí hiệu: X
– Áp dụng: từ kí hiệu nguyên tử X tính số p, e, n và ngược lại
– Nguyên tử khối là khối lượng tương đối của nguyên tử và được coi bằng số khối (A).
– Các đồng vị của cùng một nguyên tố hóa học là những nguyên tử có cùng số p nhưng khác nhau về số n Þ số khối A khác nhau Þ một nguyên tố có thể có nhiều đồng vị nên khối lượng tương đối của nguyên tử là nguyên tử khối trung bình của các đồng vị đó
– Áp dụng với đồng vị của các nguyên tố H, Cl, O, K, Ar…
Bài 4. CẤU TẠO VỎ NGUYÊN TỬ
Chuẩn kiến thức kĩ năng
Kiến thức
– Các electron chuyển động rất nhanh xung quanh hạt nhân nguyên tử không theo những quỹ đạo xác định, tạo nên vỏ nguyên tử.
– Trong nguyên tử, các electron có mức năng lượng gần bằng nhau được xếp vào một lớp (K, L, M, N).
– Một lớp electron bao gồm một hay nhiều phân lớp. Các electron trong mỗi phân lớp có mức năng lượng bằng nhau.
– Số electron tối đa trong một lớp, một phân lớp.
Kĩ năng
Xác định được thứ tự các lớp electron trong nguyên tử, số phân lớp (s, p, d) trong một lớp.
Trọng tâm
– Sự chuyển động của các electron trong nguyên tử
– Lớp và phân lớp electron
Hiểu và phân tích được:
– Các electron chuyển động rất nhanh trong khu vực xung quanh hạt nhân không theo một quỹ đạo xác định tạo nên vỏ nguyên tử.
– Vỏ nguyên tử gồm các electron chiếm các mức năng lượng khác nhau trong nguyên tử tạo nên lớp và phân lớp electron.
– Lớp e (K, L, M…) gồm các electron có mức năng lượng gần bằng nhau. Lớp K có mức năng lượng thấp nhất và gần hạt nhân nhất. Số electron tối đa trong mỗi lớp là 2n2( n là số thứ tự của lớp (1,2,3,4).
– Phân lớp electron (s,p,d, f…) gồm các electron có mức năng lượng bằng nhau. Phân lớp s có mức năng lượng thấp nhất. Số electron tối đa trong mỗi phân lớp s, p, d, f… tương ứng là 2, 6, 10, 14…
Nêu thí dụ minh họa với nguyên tử cụ thể.
Xác định số electron và biểu diễn được sự phân bố các electron trên mỗi lớp trong nguyên tử cụ thể N, Mg.
Bài 5. CẤU HÌNH ELECTRON CỦA NGUYÊN TỬ
Chuẩn kiến thức kĩ năng
Kiến thức
– Thứ tự các mức năng lượng của các electron trong nguyên tử.
– Sự phân bố electron trên các phân lớp, lớp và cấu hình electron nguyên tử của 20 nguyên tố đầu tiên.
– Đặc điểm của lớp electron ngoài cùng: Lớp ngoài cùng có nhiều nhất là
8 electron (ns2np6), lớp ngoài cùng của nguyên tử khí hiếm có 8 electron (riêng heli có 2 electron). Hầu hết các nguyên tử kim loại có 1, 2, 3 electron ở lớp ngoài cùng. Hầu hết các nguyên tử phi kim có 5, 6, 7 electron ở lớp ngoài cùng.
Kĩ năng
– Viết được cấu hình electron nguyên tử của một số nguyên tố hoá học.
– Dựa vào cấu hình electron lớp ngoài cùng của nguyên tử suy ra tính chất hoá học cơ bản (là kim loại, phi kim hay khí hiếm) của nguyên tố tương ứng.
Trọng tâm
– Thứ tự các mức năng lượng của các electron trong nguyên tử.
– Sự phân bố electron trên các phân lớp, lớp và cấu hình electron nguyên tử.
– Đặc điểm cấu hình của lớp electron ngoài cùng.
Hiểu và phân tích được:
– Biết các mức và phân mức năng lượng theo thứ tự tăng dần: 1s 2s 2p 3s… 5s có chú ý sự chèn mức năng lượng 4s và 3d.
– Nêu được quy ước cách viết cấu hình electron nguyên tử và vận dụng để viết được cấu hình electron của 20 nguyên tố đầu tiên.
– Dựa vào cấu hình electron lớp ngoài cùng của một nguyên tố, HS xác định được:
+ Đó là nguyên tố s hay p, d, s và p tùy thuộc vào vị trí của e ở lớp ngoài cùng. Nêu thí dụ minh họa.
+ Tính chất cơ bản của nguyên tố thuộc loại khí hiếm (8e) hay kim loại (thường 1e- 3e) hoặc phi kim (5e- 7e). Nêu thí dụ minh họa.
 P đỏ (hơi) → P trắng.
P đỏ (hơi) → P trắng.








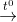 2P2O5; P2O5 + 3H2O → 2H3PO4.
2P2O5; P2O5 + 3H2O → 2H3PO4.


